在肿瘤防治研究不断深入的背景下,耐药问题已成为制约临床疗效提升的关键瓶颈,系统解析肿瘤发生发展的内在机制,特别是肿瘤微环境在疾病进程及治疗反应中的调控作用,已成为引领国际研究趋势的前沿领域和关键突破方向。
近日,兰大一院孟文勃教授团队联合重庆大学肿瘤医院李德卫教授研究团队,围绕肝外胆管癌(extrahepatic cholangiocarcinoma,eCCA)这一临床难治肿瘤,取得重要研究突破。研究首次从肿瘤微环境角度系统揭示了胆管癌化疗耐药的关键驱动机制,并提出逆转耐药的联合靶向治疗策略。相关成果论文Targeting cancer-associated fibroblast-activated HGF/c-MET pathway inhibits extrahepatic cholangiocarcinoma progression and restores gemcitabine therapeutic sensitivity,发表于国际药学领域TOP期刊Acta Pharmaceutica Sinica B 。
胆管癌是一类高度恶性的消化系统肿瘤,其中肝外胆管癌约占80%。由于其起病隐匿、进展迅速、易早期转移,绝大多数患者确诊时已处于中晚期。以吉西他滨为基础的联合化疗虽为标准治疗方案,但肿瘤耐药几乎不可避免,成为疗效提升的关键瓶颈。
针对这一临床难题,研究团队创新性构建了多层级、系统化的患者来源研究平台,涵盖原代肿瘤细胞、患者来源类器官(PDOs)、癌相关成纤维细胞(CAFs)以及患者来源异种移植模型(PDX),实现了从体外到体内、从细胞到整体的全链条肿瘤微环境重建,为深入解析胆管癌进展及耐药机制提供了重要支撑。
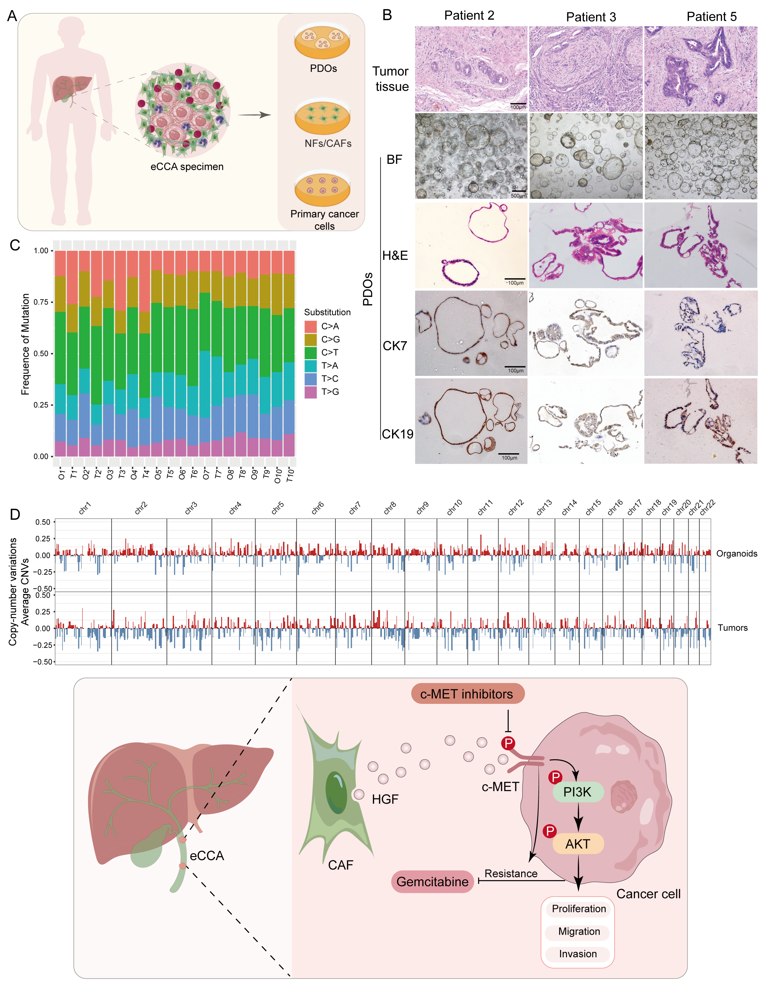
研究发现,长期被忽视的癌相关成纤维细胞(CAFs)在肝外胆管癌中并非配角,而是驱动疾病进展的重要因素。CAFs通过分泌肝细胞生长因子(HGF),显著增强肿瘤细胞的增殖、迁移与侵袭能力,并直接诱导了胆管癌细胞发生吉西他滨耐药。机制研究进一步揭示,CAF来源的HGF通过激活肿瘤细胞表面的c-MET受体,级联启动c-MET/PI3K/AKT信号通路,形成驱动肿瘤进展与化疗耐药的核心分子轴。这一发现将胆管癌耐药的研究视角由“肿瘤细胞本身”拓展至“微环境协同调控”,为实现耐药的精准干预与可逆调控提供了新的突破口。
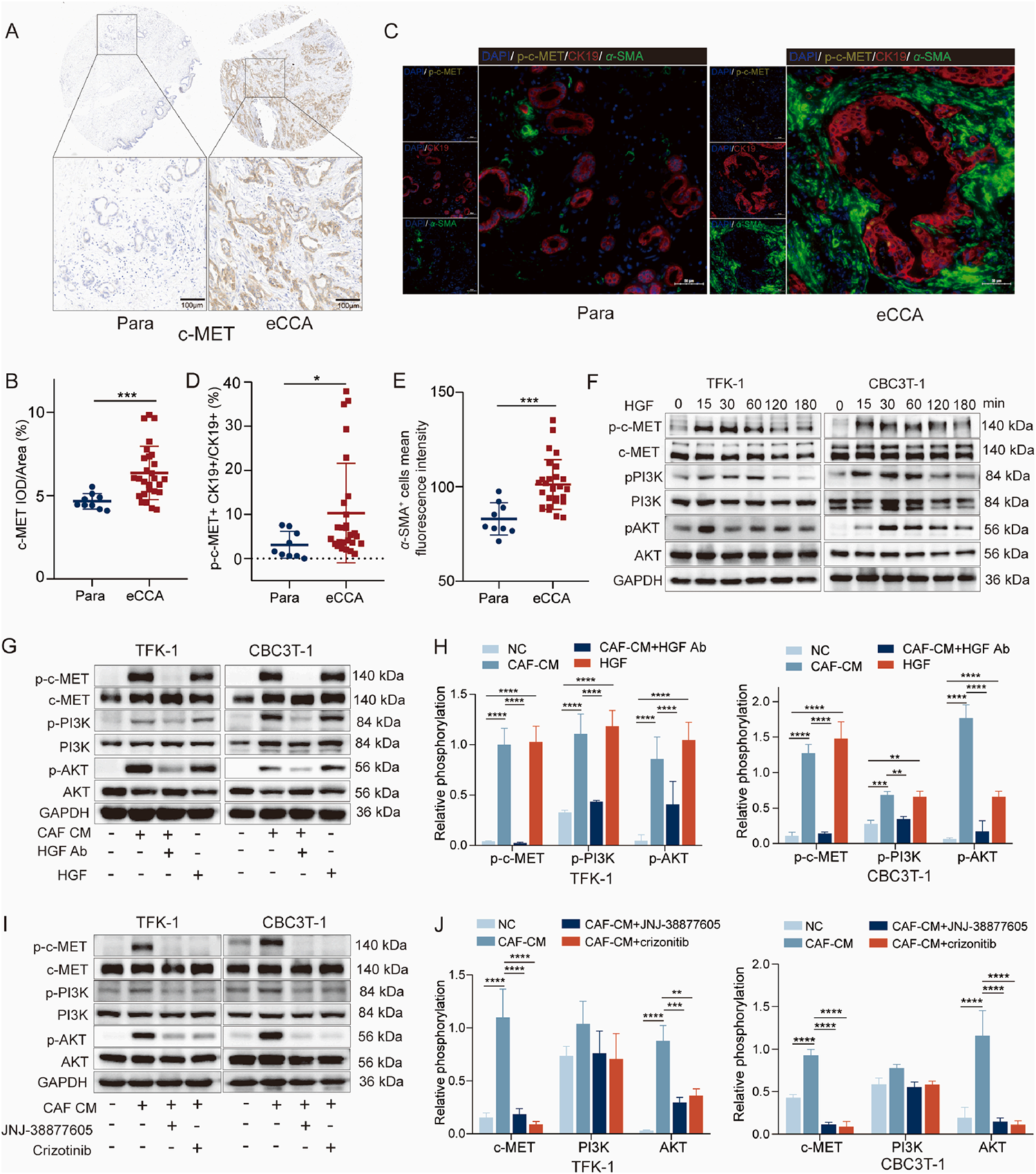
在此基础上,研究团队进一步推进研究成果向临床转化。结果表明,靶向c-MET的抑制剂不仅能够显著抑制肿瘤生长,还可在一定程度上恢复肝外胆管癌对吉西他滨的治疗敏感性。在类器官模型和PDX动物模型中,吉西他滨联合c-MET抑制剂治疗较单药方案显示出更优的抗肿瘤效果,提示胆管癌耐药有可逆性,且能够被精准干预与重塑。
该研究建立了多种胆管癌类型患者来源的细胞及类器官等研究模型,展现出面向临床重大需求的问题导向研究能力和多模型整合的技术创新优势,形成了从机制解析到治疗策略探索的完整研究路径,为提高胆管癌患者治疗的化疗敏感性、改善临床预后提供新的思路。
兰州大学第一医院(第一临床医学院)博士研究生白明圳为该文章第一作者,孟文勃教授、姚佳研究员和李德卫教授(重庆大学)为本文共同通讯作者。研究工作得到了国家自然科学基金、甘肃省科技成果转化与应用专项及甘肃省卫生健康行业科研计划项目的资助。
全文链接:https://doi.org/10.1016/j.apsb.2026.02.023
文图|普外科
编辑|党委宣传部 刘丽君
责任编辑|党委宣传部 马凌
审核|党委宣传部 陈勇





 甘公网安备 62010202000472号
甘公网安备 62010202000472号